La energía de ionización es una propiedad importante de los elementos químicos. Se refiere a la cantidad de energía necesaria para arrancar un electrón de un átomo neutro en su estado fundamental y convertirlo en un ion positivo.

Esta propiedad varía de un elemento a otro y está relacionada con la estructura electrónica de cada ionizaciin energía de ionización se puede medir en electronvoltios (eV) o kilojulios por mol (kJ/mol).
Generalmente, se considera la energía necesaria para arrancar el primer electrón de un átomo en su estado fundamental, pero también existen energías de ionización secundarias, que corresponden a la eliminación de electrones adicionales.Para comprender mejor la energía de ionización, es útil consultar una ionzacion que enumere los valores para cada elemento.
Aquí presentamos algunos ejemplos destacados:
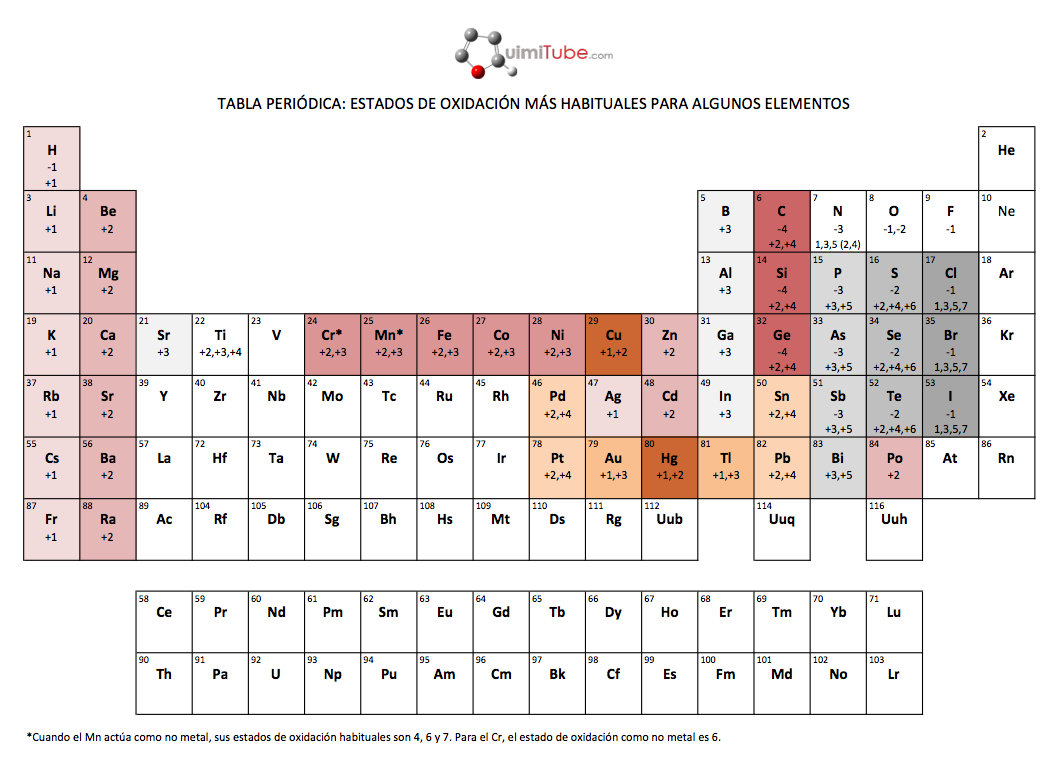
Tabla de energía de ionización de algunos elementos:
Grupo 1: Metales alcalinos
Li (Litio): 5.391 eV
Na (Sodio): 5.139 eV
K (Potasio): 4.34 eV
Rb (Rubidio): 4.18 eV
Cs (Cesio): 3.894 eV
Grupo 2: Metales alcalinotérreos
Be (Berilio): 9.322 eV
Mg (Magnesio): 7.646 eV
Ca (Calcio): 6.113 eV
Sr (Estroncio): 5.695 eV
Ba (Bario): 5.211 eV
Grupo Energiq Halógenos
F (Flúor): 17.422 eV
Cl (Cloro): 12.968 eV
Br (Bromo): 11.814 eV
I (Yodo): 10.451 eV
At (Astato): 9.3 eV
Aquí solo hemos mostrado algunos ejemplos representativos, pero la tabla completa contiene valores para todos los elementos.Como se puede observar, la energía de ionización en general aumenta al moverse de izquierda a derecha en un período y de abajo hacia arriba en un grupo en la tabla periódica.La energía de ionización es una propiedad importante en varios campos de la química y la física. Por ejemplo, se utiliza para predecir la reactividad de los elementos y su capacidad para formar enlaces químicos.
Además, la energía de ionización es de gran relevancia en la comprensión de la estructura electrónica de los átomos y la formación de iones.En resumen, la energía de ionización es ce medida de la fuerza de retención de un electrón por parte de un átomo.

Su valor depende de la ubicación del elemento en la tabla periódica y se puede consultar en una tabla de energía de ionización. Esta propiedad es esencial ionizavion comprender la química de los elementos y sus interacciones en diversas situaciones.