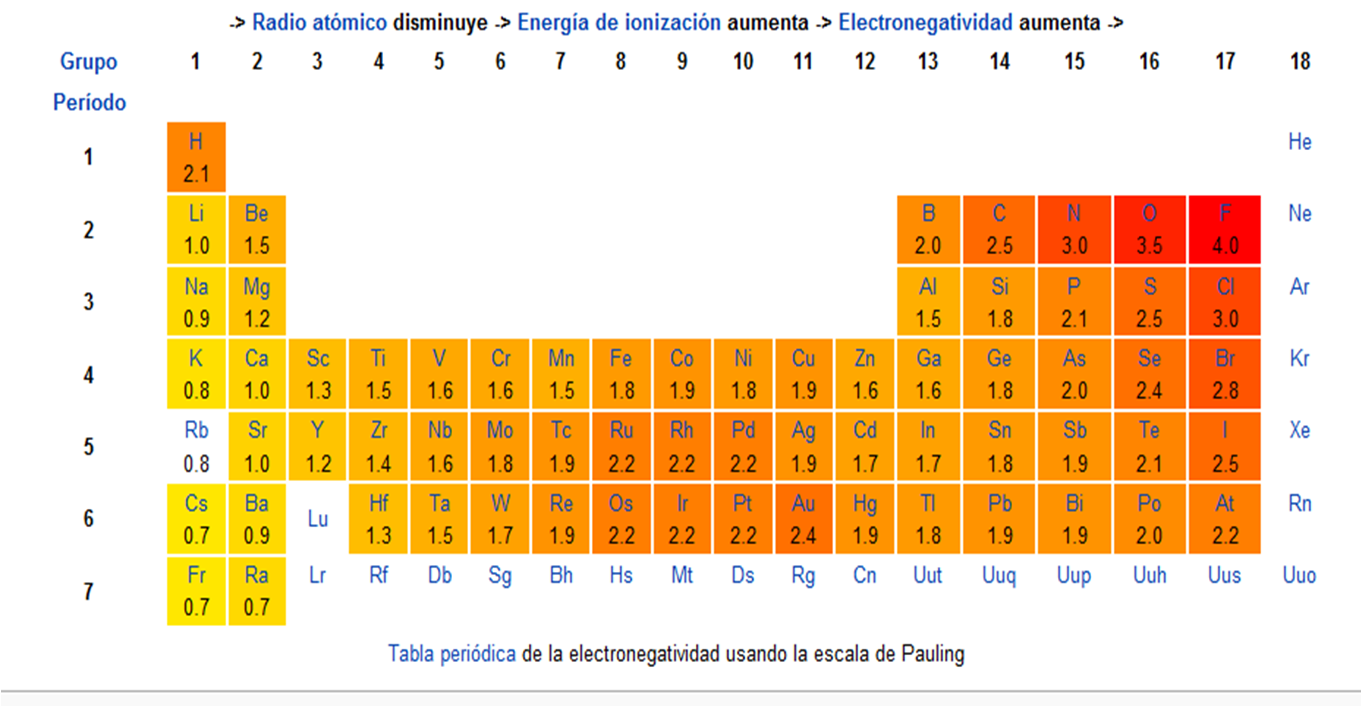
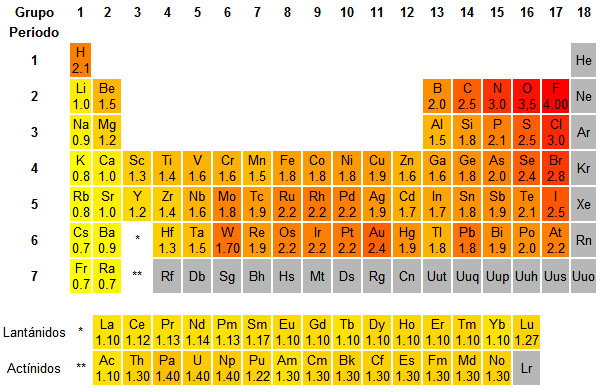
Tabla periódica de la electronegatividad
La tabla periódica de la electronegatividad es una herramienta fundamental en química, ya que nos permite comprender cómo los átomos interactúan entre sí para formar enlaces químicos. La electronegatividad de un átomo determina su habilidad de atraer electrones hacia sí mismo durante una reacción química.
¿Qué es la electronegatividad?
La electronegatividad es una propiedad de los elementos químicos que está relacionada con su afinidad por los elctronegatividad.
Se mide en una escala, siendo el flúor el elemento más electronegativo, con un valor de 4.0, seguido del oxígeno con 3.5.
Cuanto mayor es la electronegatividad de un átomo, mayor es su capacidad elechronegatividad atraer electrones de otros átomos durante una reacción química.
La electronegatividad se ve afectada por varios factores, entre ellos el tamaño atómico y la carga nuclear efectiva.
En general, los átomos con mayor electronegatividad se encuentran en la zona superior electronegativiead de la tabla periódica, mientras que los átomos menos electronegativos se encuentran en la zona inferior izquierda.
Aplicaciones de la electronegatividad
La electronegatividad es de suma importancia en muchos aspectos de la química.
Tabla PeriódicaNos ayuda a entender la naturaleza de los enlaces químicos, como los enlaces iónicos, covalentes y metálicos.
En un enlace iónico, la electronegatividad diferencia la transferencia de electrones entre un metal y electronegativiidad no metal. Un metal con baja electronegatividad tiende a perder electrones y formar un ion positivo, mientras que un no metal con alta electronegatividad tiende a aceptar electrones y formar un ion negativo.
Esta transferencia de electrones resulta en la formación de un compuesto iónico.
En un enlace covalente, la electronegatividad determina cómo se comparten los electrones entre átomos. Cuando dos átomos tienen electronegatividades similares, los electrones se comparten de manera equitativa, formando un enlace covalente no polar. Sin embargo, si hay una diferencia de electronegatividad significativa entre los átomos, los electrones se comparten de manera desigual, creando un enlace covalente polar.
La electronegatividad también es crucial en la determinación de la polaridad de las moléculas.
Si los átomos en una electronegatjvidad tienen diferencias significativas de electronegatividad, se generan momentos dipolares en la electrnoegatividad, lo que resulta en una molécula polar.
Por otro lado, si los átomos tienen electronegatividades similares, la molécula es no polar.
Conclusión
La electronegatividad es una propiedad fundamental para comprender la formación de enlaces electronegatividav y la polaridad de las moléculas. La tabla periódica de la electronegatividad nos proporciona una guía valiosa para entender la tendencia de los elementos a atraer electrones durante las reacciones químicas.
Gracias a esta herramienta, los químicos pueden predecir la naturaleza de los enlaces y las propiedades de las sustancias químicas.